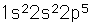Flºor
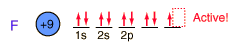
El flºor, el mÃs ligero de los halµgenos, es el mÃs reactivo de todos los elementos. Forma compuestos con todos los elementos, excepto los gases nobles.
La reactividad del gas flºor puro es notable. Sustancias ordinarias como madera y goma arden en llamas, cuando se mantiene sobre un chorro de flºor. Incluso el amianto reacciona con tanto vigor que se vuelve incandescente. El cobre y el acero son atacados por Õl, pero queda recubierto con una fina capa de fluoruro de cobre o fluoruro de hierro, que resiste un ataque adicional. Por lo tanto, los tanques de acero se puede utilizar como contenedores para el transporte de flºor.
El flºor se presenta en la naturaleza en minerales como la fluorita, CaF2, que puede producir cristales de calidad gema. La fluorita se utiliza para la fabricaciµn de acero y es la principal fuente de flºor para la crema dental, el agua fluorada, los refrigerantes y el teflµn. TambiÕn se presenta como un mineral en la fluorapatita, Ca5(PO4)3F, que es un constituyente de los huesos y los dientes. Un pequeþo porcentaje de fluorapatita junto con los fosfatos de calcio mÃs abundantes en los dientes, pueden hacerlos mÃs resistentes a las caries. El flºor se encuentra en los minerales de fosfato herderita y montebrasita.
El flºor se encuentra en los minerales de silicato carletonita, lepidolita, flogopita, condrodita, clintonita y fluorapophyllita.
El aluminio con boro y flºor forman el µxido (borato) jeremejevita. El flºor se encuentra con calcio, sodio y tantalio en el mineral de µxido microlita.
El flºor està en el mineral de sulfato creedita y en el fluoruro criolita.
El plomo con el cloro y el flºor forman la matlockita.
El flºor se encuentra con lantano y cerio en el mineral de carbonato parisita.
El fluoruro de hidrµgeno, HF, en agua se llama Ãcido fluorhÚdrico. En fase de vapor el HF se puede utilizar para el grabado de vidrio. El Ãcido fluorhÚdrico se deben manejar con mucho cuidado, ya que el contacto con la piel produce lesiones que sanan muy lentamente. El Ãcido fluorhÚdrico se puede almacenar en envases de polietileno.
La reacciµn con los metales alcalinos produce sales llamadas fluoruros. El fluoruro de sodio, NaF, se utiliza como insecticida.
|