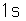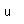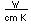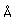Hidrógeno
El hidrógeno es el elemento más ligero y más abundante en el universo. La razón de abundancia de hidrógeno-helio es una clave importante en el proceso cosmológico. El núcleo de hidrógeno ordinario consta de un solo protón, pero también se presenta como deuterio con un protón y un neutrón. El deuterio como isótopo del hidrógeno tiene una abundancia de 1,5 x 10-4 comparado con 0,99985 del hidrógeno ordinario. Su estabilidad es notable ya que el neutrón libre es inestable, sufriendo el decaimiento beta con una semi vida de 10,3 minutos. La energía de enlace medida del deuterón es 2,2 MeV. El hidrógeno también existe como tritio, con un protón y dos neutrones pero es inestable con una semi vida de 12,32 ańos.
El hidrógeno se encuentra en la mayoría de las sustancias que constituyen la materia viva. Hay más compuestos de hidrógeno conocidos que de cualquier otro elemento, el más importante es el agua.
Es el más ligero de los gases, la densidad del hidrógeno es un catorceavo la del aire. Su punto de fusión (14 K) y su punto de ebullición (20,3 K) son más bajos que los de cualquier otro elemento excepto el helio. Como era de esperar, el hidrógeno líquido a una densidad de 0,07 gm/cm3 es el más ligero de todos los líquidos. El hidrógeno sólido cristalino con 0,088 gm/cm3 es la más ligera de todas las sustancias cristalinas (ˇmás ligero que una nube!).
En la industria se utilizan grandes cantidades de hidrógeno en la conversión de aceites (grasas líquidas) en grasas sólidas para la producción de productos alimenticios y jabones. Este proceso se llama hidrogenización
El hidrógeno tiene una mayor conductividad térmica y menor viscosidad que otros gases y se utiliza a veces en sistemas cerrados para la eliminación rápida de calor. Se ha utilizado como gas refrigerante alrededor de las armaduras de grandes generadores eléctricos.
El hidrógeno se quema en oxígeno o aire con una llama casi incolora y tiene potencial como combustible. Puesto que se requiere energía para separar hidrógeno, su potencial real es como medio de almacenamiento de energía; procesos como la electrólisis del agua puede producir hidrógeno para su almacenamiento como combustible.
El hidrógeno está en la misma columna vertical de los metales alcalinos, pero bajo las condiciones que se dan en la Tierra es un gas. Cuando se comprime extremadamente, el hidrógeno adquiere las características de un metal líquido. Las regiones profundas del interior de Júpiter y Saturno tienen condiciones de presión para producir este estado metálico líquido
|