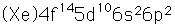Plomo
El plomo es un metal blando, pesado, de color gris mate, con resistencia a la baja tensión. Se utiliza en la fabricación de tipos, en la cobertura de cables eléctricos, y en muchas aleaciones. El principal compuesto orgánico, el tetraetilo de plomo, Pb(C2H5)4, fue ampliamente utilizado como aditivo de la gasolina, para evitar el golpe en el motor del automóvil, hasta que se suspendió su uso ante la preocupación por la toxicidad del plomo.
El plomo en el aire forma una fina capa superficial de óxido, que cambia lentamente a carbonato básico. El agua dura forma un revestimiento similar sobre el plomo, que protege el agua de una mayor contaminación con compuestos de plomo solubles. El agua blanda disuelve cantidades apreciables de plomo, que es venenoso.
El monóxido de plomo, PbO, llamado litargirio se obtiene por calentamiento de plomo en aire. Se trata de un polvo de color amarillo o rojo amarillento de material cristalino que se utiliza en la fabricación de vidrio de plomo.
El plomo rojo, Pb3O4, se puede hacer por calentamiento de plomo en oxígeno. Se utiliza en la fabricación de vidrio y en la fabricación de una pintura de color rojo -minio-, para la protección de estructuras de hierro y de acero.
El dióxido de plomo, PbO2, es ampliamente utilizado en las baterías eléctricas de plomo. La forma mineral de dióxido de plomo se llama plattnerita.
El plomo blanco -cerusa-, es un carbonato básico de plomo, Pb3(OH)2(CO3)2, que fue ampliamente utilizado como pigmento blanco en la pintura, hasta que las preocupaciones acerca de la toxicidad del plomo paralizó la mayoría de estos usos. El carbonato de plomo, PbCO3, en forma de mineral se llama cerusita. Otra forma de carbonato de plomo es la fosgenita. Un mineral de plomo con ambos grupos carbonato y sulfato es la leadhillita.
El cromato de plomo, PbCrO4, también se utiliza como pigmento con el nombre de amarillo de cromo. Un brillante color rojo-anaranjado es exhibido por el mineral, crocoita, una forma mineral de PbCrO4.
El plomo en su forma metálica es ampliamente utilizado para la protección contra la radiación, debido a su alta constante de absorción de los rayos X y los rayos gamma.
El plomo se presenta en forma natural en el mineral de sulfuro galena (PbS), y se presenta con vanadio en la vanadinita. El plomo forma un sulfuro con antimonio y hierro llamado jamesonita, y sulfuros con antimonio llamados zinkenita, plagionita, semseyita y boulangerita. La dufrenoysita y la gratonita son sulfuros de plomo con arsénico. Un sulfuro formado con antimonio y arsénico se llama jordanita. Un sulfuro formado con estańo, hierro y antimonio se llama cilindrita. La bournonita es un sulfuro de cobre, plomo y antimonio. Un sulfuro formado con estańo y antimonio se llama franckeita. El plomo se encuentra en el mineral nagyagita, un sulfuro, junto con oro, hierro, antimonio, y telurio. La plata se une con el plomo y el antimonio en el sulfuro andorita, AgPbSb3S6. El plomo, el cobre y el hierro se unen en el sulfuro betekhtinita. En el mineral de sulfuro hutchinsonita, (Tl, Pb)2As5S9, el plomo se une con arsénico y talio.
El sulfato de plomo, PbSO4, en forma mineral anglesita es a veces de calidad gema. Otro sulfato de plomo es la lanarkita.
El plomo forma un mineral de óxido de titanio, hierro y manganeso llamado senaita. Un óxido de zinc y vanadio es la descloizita. El óxido de uranio y vanadio es la francevillita. Un óxido de plomo con zinc, vanadio y cobre es la mottramita.
Un mineral de cloruro de plomo es la mendipita, PbO2Cl2.
Un cloruro de cobre y plomo es la diaboleita. Un cloruro de plomo y antimonio es la nadorita, PbSbO2Cl. El plomo con el cloro y el flúor forma la matlockita. Otros minerales de cloruro que contienen plomo son la boleita, la mimetita, la cumengita y la laurionita. El mineral de carbonato que contiene plomo, la fosgenita, tambien contiene cloro.
Una forma mineral de selenio es el compuesto de plomo, clausthalita, PbSe.
La beudantita es un mineral que contiene hierro y plomo junto con grupos sulfato y arseniato, PbFe3(AsO4,SO4)2(OH)6. Un color verde llamativo es exhibido por el mineral bayldonita que combina cobre, zinc y plomo con un grupo arseniato. La duftita es un mineral de arseniato de plomo y cobre. El mineral de fosfato piromorfita , Pb5(PO4)3Cl, también presenta un color verde aunque también aparece en tonos marrones, rojos y amarillos. El plomo se presenta con cobre en la caledonita. El plomo se presenta con uranio en la curita y la kasolita.
 |
El plomo es uno de los pocos elementos que se pueden encontrar en la naturaleza en forma pura. Esta muestra de plomo elemental con pirocroita se muestra en el Museo Smithsonian de Historia Natural. La gran muestra tiene aproximadamente 18x30 cm y proviene de Langban Mine, Filipstad, Värmland, Suecia. |
|
Índice
Tabla Periódica
Conceptos de Química
Referencia
Pauling
Cap. 26 |