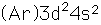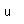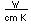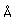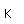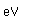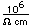Titanio
El titanio es un metal de transición muy fuerte y ligero (4.4 gm/cm3). Tiene un punto de fusión alto (1800°C) y encuentra aplicación en alas de aviones, particularmente en los puntos que están sometidos a las altas temperaturas de escape.
El dióxido de titanio en forma de polvo es muy blanco y se utiliza ventajosamente como pigmento en pinturas especiales y polvos para la cara. El dióxido de titanio, TiO2, en forma cristalina aparece en el mineral rutilo. Puede estar coloreado por pequeńas cantidades de otros óxidos metálicos, y se ha utilizado para las gemas. El dióxido de titanio también forma los minerales brookita y anatasa. El titanio y el hierro forman los óxidos, ilmenita, FeTiO3, y pseudobrookita, Fe2TiO5. El titanio y el calcio forman el óxido perovskita, CaTiO3. El titanio aparece con manganeso y arsénico en el mineral cafarsita.
El titanio se encuentra en los minerales aeschynita, euxenita y
astrofilita. El titanio forma un óxido mineral con plomo, hierro y manganeso llamado senaita. El titanio se encuentra en los minerales de silicato joaquinita y neptunita.
El tetracloruro de titanio es líquido a temperatura ambiente, pero si se pulveriza en el aire, se hidroliza para formar HCl y partículas finas de dióxido de titanio. Se ha utilizado para la fabricación de pantallas de humo. Para la "escritura del cielo" por las aeronaves, se utiliza un aerosol de tetracloruro de titanio.
|
Índice
Tabla Periódica
Conceptos de Química
Referencia
Pauling
Cap. 29 |