La Entropķa como Medida de la Multiplicidad de un Sistema
La probabilidad de encontrar un sistema en un estado determinado depende de la multiplicidad de ese estado. Es decir, es proporcional al nśmero de maneras en que se puede producir ese estado. Aquķ un "estado" es definido por alguna propiedad medible que permita distinguirlo de otros estados. En el lanzamiento de un par de dados, la propiedad medible, es la suma de la cantidad de puntos boca arriba. La multiplicidad de mostrar dos puntos es sólo uno, porque sólo hay una disposición de los dos dados que nos darį ese estado. La multiplicidad de mostrar siete puntos es de seis, porque con los dos dados hay seis arreglos que muestran un total de siete puntos.
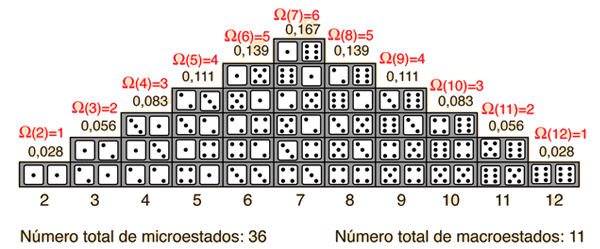
Una forma de definir la cantidad "entropķa" es hacerlo en función de la multiplicidad.
donde k es la constante de Boltzmann. Esta es la expresión de Boltzmann para la entropķa, y de hecho S = klnΩ estį tallada en su lįpida! La k se incluye como parte de la definición histórica de entropķa y proporciona las unidades Joule / Kelvin en el sistema de unidades SI. Se utiliza el logaritmo para hacer que la entropķa definida tenga un tamao razonable. También proporciona el tipo de comportamiento correcto para combinar dos sistemas. La entropķa de los sistemas combinados serį la suma de sus entropķas, pero la multiplicidad serį el producto de sus multiplicidades. El hecho de que el logaritmo del producto de dos multiplicidades sea la suma de sus logaritmos individuales, da el tipo adecuado de combinación de entropķas. La multiplicidad para colecciones ordinarias de materia es inconvenientemente grande, del orden del nmero de Avogadro, por lo que es conveniente usar para la entropķa el logaritmo de la multiplicidad
En un sistema con un gran nśmero de partķculas, como una mol de įtomos, el estado mįs probable serį abrumadoramente probable. Se puede esperar con confianza que el sistema en equilibrio, se encontrarį en el estado de mįxima multiplicidad, ya que por lo general, las fluctuaciones de ese estado serįn demasiado pequeńas para ser medidas. Cuando un sistema grande alcanza el equilibrio, su multiplicidad (entropķa) tiende a aumentar. Esta es una forma de establecer la segunda ley de la termodinįmica.
Conceptos de Entropķa
Referencia
Schroeder
Cap. 2
| HyperPhysics*****Termodinįmica | M Olmo R Nave |