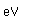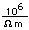Aluminio
El aluminio es un metal abundante, ligero y fuerte que ha encontrado muchos usos. El principal inconveniente de su uso es la gran cantidad de energía necesaria para refinarlo a partir de su mineral común, la bauxita. El reciclaje de la chatarra de metal de aluminio ahorra más del 90% de la energía requerida para separar el aluminio de la bauxita.
El aluminio tiene solamente alrededor de un tercio de la densidad del hierro, pero algunas de sus aleaciones, tales como el duraluminio son tan fuertes como el acero dulce. El duraluminio se forma con aluminio 94,3%, el 4% de cobre, el 0,5% de manganeso, el 0,5% de magnesio, y el 0,7% de silicio. Aunque mucho más fuerte que el aluminio puro, esta aleación es menos resistente a la corrosión y es a menudo revestido con aluminio puro.
Debido a su ligereza y resistencia, el aluminio se utiliza ampliamente en la construcción de aviones. Tiene una alta conductividad eléctrica, el 80% de la del cobre, y se utiliza en lugar del cobre en grandes conductores eléctricos. Su desventaja es su tendencia a oxidarse en los contactos, lo que requiere el uso de contactos revestidos con un antioxidante.
El aluminio es un metal muy activo, un hecho a menudo disimulado porque se forman rápidamente barreras de capas de óxido en las superficies expuestas, inhibiendo su interacción. Cuando se calienta fuertemente se quema rápidamente en el aire, y en la forma de polvo fino es explosivo.
El aluminio es uno de los 8 grandes elementos en la corteza terrestre, siendo el tercer elemento más abundante, alrededor del 8,1% en peso. Es un componente de la clase de los silicatos llamados feldespatos, que son los minerales más abundantes en la corteza terrestre. Es también un constituyente de la mica. La pirofilita, AlSi2O5(OH), es un mineral de silicato de aluminio. El aluminio se combina con otros metales en muchos silicatos, por ejemplo, manganeso en la espesartina, Mn3Al2(SiO4)3. Un silicato de aluminio, Al2SiO4 (F,OH)2, constituye la joya mineral topacio. Un silicato de potasio, KAlSi3O8, forma el mineral microclina, que puede tener el color desde verde manzana hasta marrón. Un silicato con calcio, la zoisita forma las gemas azules. El silicato de aluminio cianita forma cristales azules que pueden tener calidad de gema. Otros silicatos de aluminio de litio son, el espodumeno, LiAlSi2O9 y la petalita, LiAlSi4O10.
El óxido de aluminio, Al2O3, se llama alúmina, y se produce en la naturaleza en el mineral corindón. El corindón y el corindón impuro llamado esmeril, se utilizan en la fabricación de papeles abrasivos (lijas) y ruedas (piedras esmeril). El corindón puro es incoloro, pero la adición de una pequeńa impureza de óxido de cromo puede hacer la piedra preciosa rubí (rojo), y la adición de óxido de titanio puede hacer el zafiro (azul y otros colores). Otro óxido de aluminio es el diásporo, AlO(OH).
El aluminio junto con el magnesio forman la espinela, óxido mineral. El aluminio con el zinc constituyen la gahnita, óxido mineral. El aluminio con boro y flúor forman el óxido, (borato), jeremejevita.
Un mineral de fosfato de aluminio es la variscita, AlPO4.2H2O, que presenta un color verde manzana y es popular como piedra ornamental. Otro mineral de fosfato de aluminio es la Brasilianita, que también puede tener calidad de gema. El aluminio aparece con el magnesio y el hierro en el fosfato lazulita. La paravauxita es un fosfato de aluminio y hierro.
El sulfato de aluminio se utiliza en la purificación del agua. También se utiliza como mordiente en el tintado de tela. El mordiente fija el tinte a la tela, haciéndolo insoluble.
El aluminio tiene excelentes propiedades reflectoras y es ampliamente utilizado en los recubrimientos por evaporación en la fabricación de espejos.
|
Índice
Tabla Periódica
Conceptos de Química
Referencia
Pauling
Cap. 26
Schad
Cap. 15 |