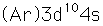Cobre
El cobre es un metal rojo, Ãspero, con un punto de fusiµn moderadamente alto. Es un excelente conductor del calor y de la electricidad y encuentra un amplio uso como conductor elÕctrico.
El cobre puro es blando y puede ser convertido en alambre o moldeado en las formas deseadas. Estos procesos de conformaciµn hacen que el metal se vuelva duro, porque los grandes granos de cristal se descomponen en pequeþos granos, fortaleciendo el metal. Si el cobre es posteriormente calentado (recocido), se puede volver de nuevo blando.
El latµn està formado por una aleaciµn de cobre y zinc. Si se aþade estaþo, se obtiene el bronce. Las aleaciones de cobre y aluminio son llamadas bronce de aluminio.
El sulfato de cobre (CuSO4.5H20) es un compuesto comºn de cobre. El sulfato de cobre se utiliza en el chapado de cobre, en la impresiµn de telas, y en las cÕlulas elÕctricas. Los nombres comunes son vitriolo azul y piedra azul.
El cobre metÃlico aparece en la naturaleza en una variedad de formas minerales. Aparece con magnesio en el mineral de carbonato callaghanita. El mineral de carbonato malachita tiene un rico color verde oscuro que lo hace un material decorativo ampliamente utilizado. Su carbonato compaþero la azurita, tiene un intenso color azul.
La cuprita es la forma mineral del µxido Cu2O. Otro µxido de cobre mas raro es la paramelaconita, Cu4O3. El cobre forma un µxido de hierro llamado delafossita. Un µxido de cobre con zinc, vanadio y plomo es la mottramita.
El cobre forma los sulfuros covellita, CuS, calcocita, Cu2S, y digenita, Cu9S5. Con hierro forma la calcopirita, CuFeS2, con antimonio forma la calcostibita, CuSbS2 y con arsÕnico forma la calcofilita. El cobre tambiÕn forma un sulfuro con bismuto llamado emplectita, CuBiS2. Forma un sulfuro con antimonio y hierro llamado tetrahedrita.
Los sulfuros con hierro incluyen la bornita, Cu5FeS4, y la cubanita, CuFe2S3. Un sulfuro con arsÕnico se llama enargita. La bournonita es un sulfuro con cobre, plomo y antimonio. La tennantita es un sulfuro que contiene cobre, arsÕnico, hierro y antimonio. El plomo, cobre y hierro se juntan en el sulfuro betekhtinita. La germanite es un sulfuro que contiene cobre, germanio y hierro. La stannita es un sulfuro con estaþo y cobre. El cobre con plata y antimonio forma el sulfuro polybasita.
Se presenta en forma de sulfato en la antlerita, la brochantita, la connellita, la cyanotrichita y la devillina.
El cobre aparece con plomo en la caledonita. El cobre, el cobalto y el nÚquel se unen en el sulfuro carrollita. Un color verde llamativo es exhibido por el mineral bayldonita que combina cobre, cinc y plomo con un grupo arseniato. Otro mineral de cobre verde es el arseniato de cobre olivenita, Cu2AsO4(OH). Otro arseniato de cobre es la clinoclasa. La duftite es un mineral arseniato de plomo y cobre. El silicato de cobre en el mineral dioptasa tambiÕn exhibe un color verde. La dioptasa està a veces acompaþada por un raro silicato de cobre, la plancheita. El cobre aparece como cloruro en la atacamita, la boleita y la cumengita. Un cloruro de cobre y plomo es la diaboleita. El cobre aparece como un fosfato en la cornetita.
El cobre constituye el mineral de fosfato libethenite. El cobre aparece con uranio en el mineral de fosfato metatorbernita.
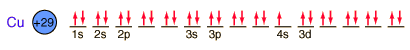
El cobre es una de las pocas excepciones a la orden de llenado general de los orbitales electrµnicos, llenando los diez estados 3d antes de llenar el segundo estado 4s.
|
ëndice
Tabla Periµdica
Conceptos de QuÚmica
Referencia
Pauling
Cap. 28 |