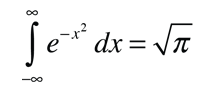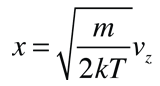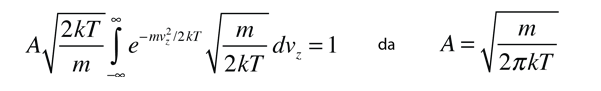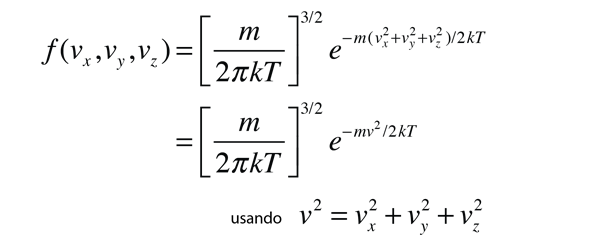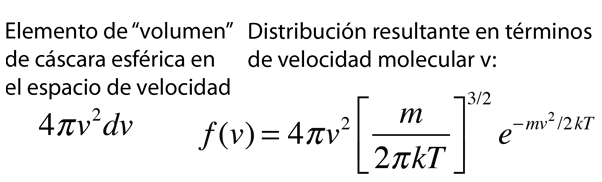Distribuciµn de Velocidades de Maxwell Directamente de la Distribuciµn de Boltzmann
La distribuciµn de Boltzmann es fundamental para nuestra comprensiµn del fenµmeno molecular clÃsico, que nos dice que la probabilidad de encontrar una molÕcula cualquiera con una energÚa E, disminuye exponencialmente con la energÚa, es decir una molÕcula cualquiera es muy poco probable que agarre mucho mÃs que la cuota media de la energÚa total disponible para todas las molÕculas. MatemÃticamente, la distribuciµn de Boltzmann se puede escribir en la forma
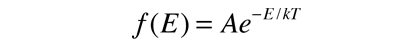
Esta distribuciµn se puede hacer posible mediante un ejemplo numÕrico, particularmente cuando se pone en forma grÃfica, pero el desarrollo matemÃtico riguroso de Boltzmann se mantiene como un importante logro en las matemÃticas de la fÚsica. Vamos a tomarlo como un postulado aquÚ y demostrar que la distribuciµn de velocidades de Maxwell se desprende de ella.
Si esta distribuciµn se aplica a una sola direcciµn de la velocidad de una molÕcula en un gas ideal, viene a ser
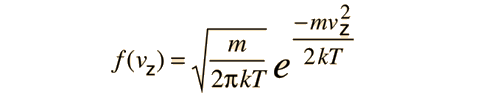 |
|
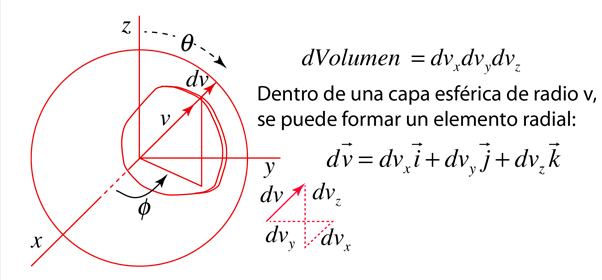
La conversiµn de esta fµrmula en otra que exprese la probabilidad en funciµn de las velocidades en tres dimensiones, da como resultado la distribuciµn de velocidades de Maxwell:
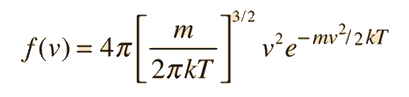
Los pasos a seguir en esta conversiµn son
| Conversiµn a Probabilidad en tres Dimensiones |
| Suma sobre todas las Direcciones Espaciales |
Conceptos sobre TeorÚa CinÕtica
| HyperPhysics*****Calor y TermodinÃmica | M Olmo R Nave |