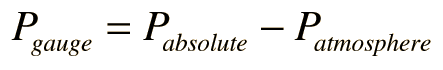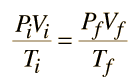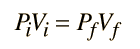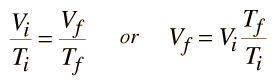Ley de Gas Ideal
Se define como gas ideal, aquel donde todas las colisiones entre átomos o moléculas son perfectamente elásticas, y en el que no hay fuerzas atractivas intermoleculares. Se puede visualizar como una colección de esferas perfectamente rígidas que chocan unas con otras pero sin interacción entre ellas. En tales gases toda la energía interna está en forma de energía cinética y cualquier cambio en la energía interna va acompańada de un cambio en la temperatura.
Un gas ideal se caracteriza por tres variables de estado: la presión absoluta (P), el volumen (V), y la temperatura absoluta (T). La relación entre ellas se puede deducir de la teoría cinética y constituye la

- n = número de moles
- R = constante universal de gas = 8.3145 J/mol K
- N = número de moléculas
- k = constante de Boltzmann = 1.38066 x 10-23 J/K = 8.617385 x 10-5 eV/K
- k = R/NA
- NA = número de Avogadro = 6.0221 x 1023 /mol
La ley del gas ideal puede ser vista como el resultado de la presión cinética de las moléculas del gas colisionando con las paredes del contenedor de acuerdo con las leyes de Newton. Pero tambien hay un elemento estadístico en la determinación de la energía cinética media de esas moléculas. La temperatura se considera proporcional a la energía cinética media; lo cual invoca la idea de temperatura cinética. Una mol de gas ideal a TPE (temperatura y presión estándares), ocupa 22,4 litros.
| Cálculo |
| Diferencia con un Gas Ideal: Ecuación de Estado de Van der Waals |
Conceptos de Gas Ideal
Conceptos de Teoría Cinética
| HyperPhysics*****Termodinámica | M Olmo R Nave |