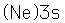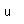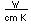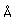Sodio
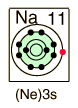 |
El sodio, al igual que los otros metales alcalinos (Grupo I), es un metal blanco plateado de muy elevada reactividad química.
El sodio es uno de los 8 grandes elementos en la corteza terrestre, siendo el sexto elemento más abundante, con aproximadamente un 2,8% en peso. Es un componente de la plagioclasa, una forma de feldespato, uno de los minerales más abundantes en la tierra. |
El compuesto de sodio más importante es el cloruro sódico, NaCl (la sal de mesa común). Cristaliza en forma de cubos incoloros. Constituye el 3% del agua del mar y también se presenta en grandes depósitos sólidos y salmueras de sal subterráneas. El NaCl es un mineral abundante. En forma cristalina se le da el nombre mineral de halita. Es importante como electrolito en la sangre y el plasma humanos, que contienen aproximadamente un 0,9 gramos de NaCl por 100 ml.
El cloruro de sodio se utiliza para la extracción de sodio metálico y cloro gaseoso, así como para la preparación de otros compuestos de estos elementos.
Los boratos de sodio, tales como el bórax (tetraborato de sodio decahidrato, Na2B4O7. 10H2O), la kernita (tetraborato de sodio tetrahidratado, Na2B4O7. 4H2O), y la colemanita (hexaborato de calcio pentahidratado, Ca2B6O11. 5H2O) forman grandes depósitos de boro en California.
El hidróxido de sodio (NaOH) es un reactivo de laboratorio muy importante y un producto químico industrial ampliamente utilizado. Llamado sosa cáustica, es muy corrosivo para la piel. Se utiliza en la fabricación de jabón, en el refinado de petróleo, la fabricación de papel, textiles, rayón, película de celulosa, y muchos otros productos.
Las propiedades del sodio metálico líquido, lo hace útil como refrigerante en los reactores reproductores rápidos, y como agente de transferencia de calor para las reacciones de muy alta temperatura.

|
Índice
Tabla Periódica
Conceptos de Química
Referencia
Pauling
Cap. 26 |