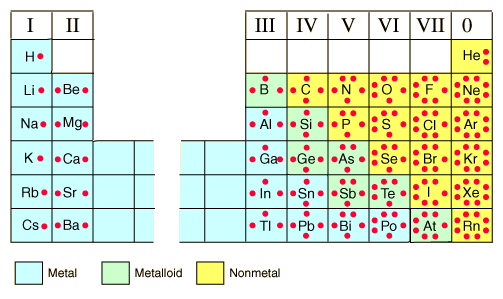
Distribución de los Electrones en Capas para los Tres Primeros Periodos
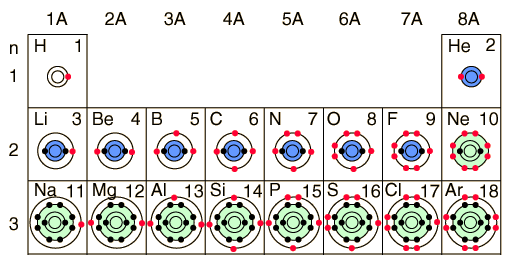
Un elemento químico se identifica por el número de protones en su núcleo, y debe tener un número igual de electrones si se desea que sea eléctricamente neutro. Cuando se agregan electrones, llenarán las capas de electrones en un orden determinado por la configuración que le de la energía más baja posible. La primera capa (n = 1) puede tener solamente 2 electrones, de modo que la capa se llena en el helio, el primer gas noble. En la tabla periódica, los elementos están colocados en "períodos" y ordenados de izquierda a derecha en el orden de llenado de los electrones de la capa exterior. Así que el hidrógeno y el helio completan el primer periodo.
El número de electrones en una determinada capa puede predecirse a partir de los números cuánticos asociados con esa capa, junto con el principio de exclusión de Pauli. La segunda capa, asociada con el número cuántico principal n=2, puede tener un máximo de 8 electrones y se corresponde con el segundo período de la tabla periódica. La tercera capa también cuenta con 8 electrones, pero las cosas se complican ahora, porque las subcapas se esparcen lo suficiente hacia fuera, para que exista un solapamiento entre ellas.
|
Índice
Conceptos de Química
Química de los Elementos
Tabla Periódica |