Elementos de Transiciµn
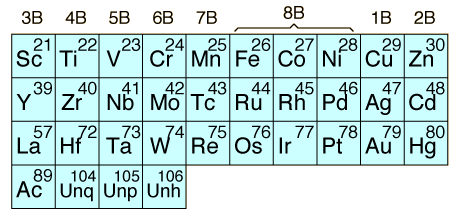
Los elementos de transiciµn son aquellos que tienen la subcapa d o f parcialmente llena en cualquier estado de oxidaciµn comºn. El tÕrmino "elementos de transiciµn" se refiere mÃs comºnmente a los elementos de transiciµn del bloque d. Los elementos 2B, zinc, cadmio y mercurio no cumplen estrictamente las caracterÚsticas que los definen, pero normalmente se incluye con los elementos de transiciµn, debido a sus propiedades similares. Los elementos de transiciµn del bloque f son a veces conocidos como "elementos de transiciµn interna". La primera fila de ellos se llama lantÃnidos o tierras raras. La segunda fila se compone de los actÚnidos. Todos los actÚnidos son radiactivos y los que estÃn por encima de Z=92 estÃn hechos por el hombre en los reactores nucleares o aceleradores.
Las propiedades generales de los elementos de transiciµn son:
- Por lo general son metales de alto punto de fusiµn.
- Tienen varios estados de oxidaciµn.
- Generalmente forman compuestos coloreados.
- A menudo son paramagnÕticos
Los elementos de transiciµn incluyen los importantes metales hierro, cobre y plata. El hierro y el titanio son los elementos de transiciµn mÃs abundantes. Muchos catalizadores para las reacciones industriales implican elementos de transiciµn.
| QuÚmica de los Elementos |
Tabla Periµdica
Conceptos de QuÚmica
Referencia
Ebbing
Cap. 23
| HyperPhysics | M Olmo R Nave |