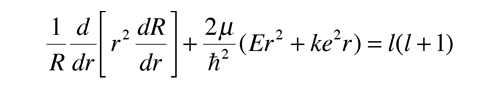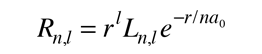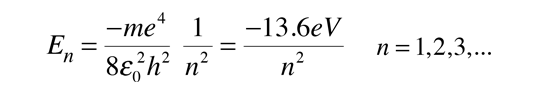Separaciµn de la ecuaciµn Radial
Sustituyendo la fµrmula
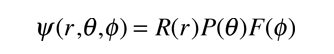
en la ecuaciµn de Schrodinger del hidrµgeno, permite expresar todas las derivadas parciales, como derivadas ordinarias. Por sustituciµn directa y un poco de reagrupamiento, da
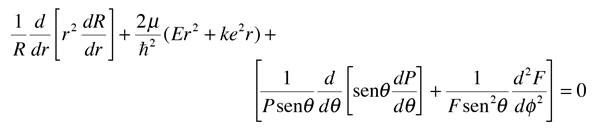
TÕngase en cuenta que los dos primeros tÕrminos sµlo contienen la variable r, y los tÕrminos restantes contienen las variables angulares. Puesto que la ecuaciµn debe ser vÃlida para todos los valores de estas variables, la colecciµn de los tÕrminos radiales debe ser igual a una constante. Esto separa la ecuaciµn radial. La suma de los tÕrminos angulares por lo tanto, debe ser igual al negativo de la constante. Asimismo, los tÕrminos de los dos Ãngulos por separado, deben ser igual a una constante, ya que deben mantenerse vÃlidos para todos los valores del Ãngulo. Esto separa las dos partes angulares, en las ecuaciones de colatitud y azimutal.
Conceptos de la Ecuaciµn de Schr—dinger
Conceptos del Hidrµgeno
| HyperPhysics*****FÚsica CuÃntica | M Olmo R Nave |