Potenciales de Electrodo y Constantes de Equilibrio
El potencial de una célula voltaica, es una medida de la cantidad mįxima de energķa por unidad de carga que estį disponible para realizar trabajo, cuando la carga se transfiere a través de un circuito externo. Este trabajo mįximo es igual al cambio en la energķa libre de Gibbs, ΔG, en la reacción. Estas relaciones se pueden expresar como
Trabajo mįximo = ΔG = -nFE°célula
donde n es el nśmero de electrones transferidos por mol y F es la constante de Faraday.
Este cambio de energķa libre también puede estar relacionado con la constante de equilibrio K
ΔG = -RT ln K
La combinación de estas relaciones nos permite expresar el potencial de célula en términos de la constante de equilibrio.
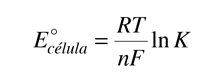
Considérese la histórica pila Daniell en el que se utilizaban zinc y cobre como electrodos. Los datos de la tabla de potenciales de electrodo estįndar es
| Cįtodo (reducción) Semirreacción | Potencial estįndar E°(voltios) |
| Zn2+(aq) + 2e- → Zn(s) | |
| Cu2+(aq) + 2e- → Cu(s) |
El potencial de célula estįndar es entonces E°célula = 1,1 voltios y se transfieren 2 electrones por mol de reactivo. La relación de la constante de equilibrio es entonces

Este extremadamente alto valor de la constante de equilibrio confirma que la reacción de la célula de Daniell es de hecho espontįnea, y que va a proseguir hasta que se agoten los reactivos.
| Tabla de Potenciales de Electrodos Estįndares |
Conceptos de
Oxidación/
Reducción
Conceptos de Electronegatividad
Referencias
Hill & Kolb
Cap. 8
Ebbing
Cap. 19
| HyperPhysics*****Electricidad y Magnetismo*****Quķmica | M Olmo R Nave |