Estructura Molecular por el Espectro de Rotación
Supongamos que se está interesado en la estructura de una molécula como el difluoruro hidrotiofosforilo que se muestra abajo. La forma más exacta para determinar la estructura molecular de una molécula en fase gaseosa es por el análisis del espectro de rotación.
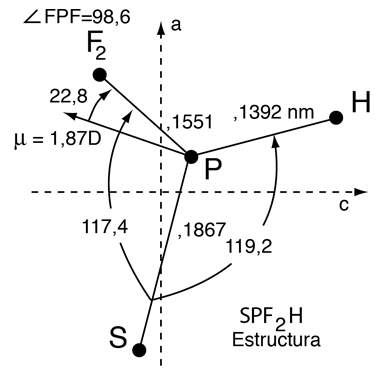
|
Conceptualmente, la historia de la determinación de la estructura molecular comienza con la expresión de la energía cinética de rotación de un rotor rígido: 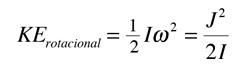 Cuando se aplica esto a una simple molécula diatómica o lineal, esta expresión de la energía cinética conduce al hamiltoniano de la mecánica cuántica  que da los valores propios de la energía. 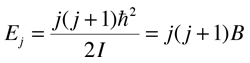 |
El parámetro B se denomina constante de rotación y es conveniente para analizar el espectro de rotación en términos de esta constante de rotación. El análisis del espectro proporciona un valor para I, y esto permite calcular la longitud del enlace de una molécula diatómica (véase el ejemplo del HCl).
Para una molécula en general, hay tres momentos de inercia no equivalentes, y la expresión de la energía cinética se convierte en
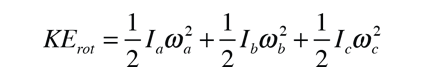
y las energías se expresan en términos de tres constantes de rotación A, B y C.
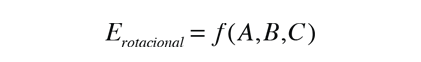
La complejidad de las expresiones de la energía es una mala noticia en cuanto a la dificultad de análisis, pero una buena noticia en términos de la información obtenida. La estructura de una molécula diatómica tiene una sola incógnita, pero cuando se tiene múltiples longitudes y ángulos de enlace, se tiene varias incógnitas y se necesitan varias ecuaciones para resolverlas.
Para determinar la estructura del SPF2H, se tiene que determinar tres ángulos y tres longitudes de enlace, por lo que se necesitan seis ecuaciones. La rotación alrededor de tres ejes independientes da tres ecuaciones. De modo que, żcómo se determina la estructura?
La idea física que nos rescata del dilema de la escasez de datos, es la sustitución isotópica. Dado que las longitudes de enlace se determina por la fuerza electrostática, la sustitución de un isótopo diferente en el átomo no debe cambiar las longitudes de enlace, ya que el entorno eléctrico alrededor del isótopo es idéntico. Sin embargo, los momentos de inercia cambiarán, dándonos tres piezas más de datos en forma de nuevas constantes rotacionales A', B', y C'.
Cuando se hizo el experimento con el SPF2H, que tiene seis parámetros estructurales, parecía que la producción de la molécula con deuterio sustituido por hidrógeno normal, sería suficiente para la determinación de la estructura, ya que nos daría 6 parámetros. Estábamos trabajando en un laboratorio de la University College de North Wales en Bangor, en Gales, sobre una muestra preparada por R. G. Cavell del Departamento de Química, Edmonton, Alberta. Esto fue unos meses después de la primera vez que el compuesto fué sintetizado. Habíamos leído sobre su síntesis inicial. Estuvimos en contacto con él y amablemente accedió a sintetizar la molécula con deuterio sustituido por hidrógeno. La molécula es muy inestable y explosiva en contacto con el aire, por lo que la muestra con deuterio fué tratada con gran cuidado y se tomaron los datos sobre su espectro durante aproximadamente dos semanas. Por desgracia, una noche, el sistema de vacío de vidrio tuvo una fuga, y cuando entramos a la mańana siguiente, encontramos que había estallado y se había perdido tanto la muestra como el sistema de vacío. Al menos tuvimos dos semanas de espectros y tuvimos datos suficientes para determinar las constantes rotacionales.
Desafortunadamente, nuestro consuelo por haber recogido suficientes datos para determinar los parámetros de las especies de moléculas con deuterio fue de corta duración, ya que nos enfrentamos a un nuevo obstáculo para la determinación de la estructura molecular. ˇSeis piezas de datos no fueron suficientes para determinar la estructura de esta molécula! Hay un plano de simetría en esta molécula, los dos átomos de flúor están en lugares que son imágenes especulares a cada lado del plano formado por el marco SPH. Esto significó que una vez que se determinaron los dos momentos de inercia en el plano de SPH, el tercer momento de inercia se determinó por el teorema del eje perpendicular, y no independientemente de los otros dos momentos de inercia. Estábamos abligados a tener seis piezas independientes de datos para calcular la estructura de forma inequívoca, y ahora sólo teníamos cuatro.
Fuimos rescatados en este caso, por el hecho de que el espectro del SPF2H era extremadamente fuerte y bien resuelto, y de hecho pudimos recoger datos para una tercera especie isotópica, las especies con azufre-34. Se tiene una abundancia natural del 3% y esto resultó ser suficiente para detectarlo. Sabíamos dónde buscar porque pudimos hacer un modelo bastante preciso con los datos de la muestra normal y con deuterio, y todavía teníamos la muestra original. Resolviendo los momentos de inercia de nuestro modelo, se predijo la ubicación de una docena o así de líneas críticas, y se buscaron en alta resolución. El tercer conjunto de constantes rotacionales A", B" y C", nos dio los datos necesarios para el cálculo de la estructura que se muestra.
|
|
Conceptos de Espectro Molecular
Referencias
Nave & Sheridan
Cavell
| HyperPhysics*****Física Cuántica | M Olmo R Nave |